En quoi la radiothérapie peut- elle permettre de soigner les cancers tout en présentant des risques d’effets secondaires ?
I) les rayonnements ionisants
1) Les différents types de rayons ionisants utilisés en radiothérapie.
Les appareils utilisés en radiothérapie peuvent délivrer plusieurs types de rayonnements ionisants.
Ils peuvent émettre:
- des particule:
- α (alpha) : particule chargée composée de deux protons et de deux neutrons. Il s’agit d’un noyau d’atome d’hélium.
Son pouvoir de pénétration demeure très faible mais elle est fortement ionisante. - β- (béta) : particule chargée négativement puisqu’il s’agit d’un électron. Son pouvoir de pénétration dépend de sa vitesse d’émission.
- neutron : particule non chargée qui peut pénétrer profondément dans la matière.
- proton : particule chargée positivement qui endommage très peu les tissus traversés avant la tumeur. Lorsqu’ils sont utilisés,
on parle de protonthérapie. - Des ondes électromagnétiques
- Si l'énergie cinétique transférée par l'électron incident (EI = 1/2mv2) est supérieure à l'énergie de liaison EL d'un électron de l'atome cible, (EI EL), alors cet électron sera expulsé du cortège électronique et une ionisation de l’atome cible se produira.
- Si l'énergie transférée par l'électron incident (Ec) est exactement égale à la différence entre les énergies de liaison de deux couches électroniques de l'atome cible (Ec = EL – EM), un électron saute sur une couche périphérique de niveau d’énergie inférieur. Il y a alors excitation de l’atome cible.
- 40 lésions « double brin » (ruptures des deux chaînes de l’ADN) ;
- de 500 à 1 000 lésions « simple brin » (ruptures d’une seule chaîne) ;
- de 1 000 à 2 000 lésions de bases azotées ;
- et environ 200 pontages (ADN-ADN ou ADN-protéine).
- une ionisation : Si l’énergie apportée par une radiation est supérieure à 5,16 eV (énergie de la liaison H-OH), alors la molécule d’eau se dissocie. H2O rayonnement HO + H (dissociation en radicaux libres)
- une excitation Si l’énergie apportée par une radiation ne dépasse pas l’énergie de liaison, la molécule d’eau se trouve excitée. Un ou plusieurs électrons se trouvent à des niveaux d’énergie plus élevés que l’état fondamental.
L’énergie cinétique de ces particules se calcule avec la formule suivante :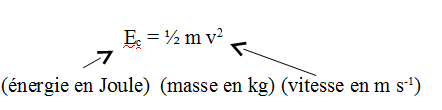
Remarque 1 : Certaines particules sont obtenues à partir de la désintégration d’éléments radioactifs ou radioéléments, produits ou naturels. C’est le cas par exemple de l’iode 131 qui en se désintégrant émet dans un premier temps un rayonnement de type β- :
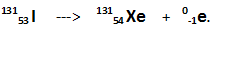
Remarque 2 : Un autre type de particules est actuellement en cours de test : les ions carbone. Un centre spécialisé en carbonethérapie (hadronthérapie) pourrait prochainement ouvrir ses portes à Lyon : le centre Etoile.
Il peut s’agir de rayons γ (gamma), X ou de photons. Leur longueur d’onde ? courte leur confère une énergie très importante et un pouvoir de pénétration dans les tissus pouvant aller jusqu’à plusieurs dizaines de centimètres. Ces ondes n’ont ni masse ni charge. Leur énergie se calcule avec l’une des deux formules suivantes :

2) Ionisation et absorption d’énergie par des atomes cibles soumis à des radiations.
Principe général : L’ionisation survient lorsque des rayonnements incidents transfèrent assez d’énergie à des atomes cibles pour leur arracher un ou des électrons. Les atomes privés de certains de leurs électrons se trouvent alors chargés positivement tandis que d’autres atomes voisins accueillent ces électrons et se chargent négativement. On assiste ainsi à la formation d’ions positifs et négatifs. Des rayonnements capables de provoquer de telles réactions sont dits ionisants.
Quels phénomènes physiques sont observés lorsqu’un atome cible est soumis à une radiation ?
►Ionisations envisagées lors d’une interaction « photon – matière (atome cible) »
L’effet photoélectrique
L’effet photoélectrique désigne l’émission d’électron(s) par un atome soumis à des photons dont l’énergie apportée (EI = h nu) dépasse l’énergie de liaison (EL) de l’électron au noyau de l’atome cible. Par exemple, pour l’atome d’oxygène, l’énergie de liaison de la couche K est de l’ordre de 1 keV (1 000 électronvolts)
Si l'énergie du photon incident est inférieure à l'énergie de liaison d’un électron de la couche K mais supérieure à l'énergie de liaison d’un électron de la couche L, alors l'effet photoélectrique se produit avec un électron de la couche L.
Dans l’exemple donné ci-dessous, un atome d’aluminium absorbe un photon gamma (γ). Un électron de la couche K se trouve éjecté.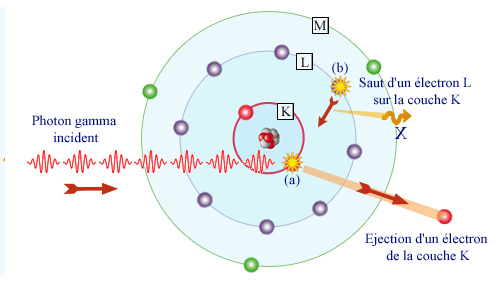
Cet atome qui vient de perdre un électron se trouve excité et très instable. Pour combler cette lacune, une réorganisation du cortège électronique va avoir lieu. Un électron d’une couche plus externe (L dans notre exemple) va alors occuper la lacune laissée par l’électron éjecté (couche K). Lors de cette transition, un photon de fluorescence (X) ou un autre électron encore plus périphérique (électron Auger) peuvent être émis.
L’effet Compton
Un photon incident interagit encore ici avec un électron, mais cet électron a une énergie de liaison beaucoup faible que celui impliqué dans l'effet photoélectrique.
L’effet Compton se caractérise par l’éjection d’un électron associé à l’émission d’un photon (photon diffusé) suivant une direction défini par un angle particulier.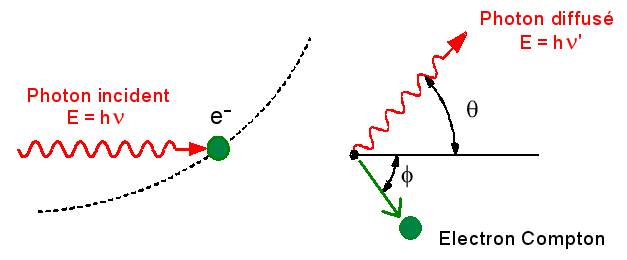
L’énergie du photon incident (EI) absorbée se répartit donc entre l'électron éjecté (Ec) et le photon diffusé (E).
Lorsque l'énergie du photon incident augmente, l'énergie cinétique emportée par l'électron Compton devient de plus en plus importante par rapport à celle du photon diffusé.
Remarque : L’effet photoélectrique et l’effet Compton conduisent tous deux à un phénomène d’ionisation. Cependant, l’effet Compton doit être maîtrisé et limité pour éviter des émissions d’électrons dans des directions non souhaitées et dangereuses aussi bien pour les patients que pour le personnel médical.
►scénarios envisagés lors d’une interaction « électron (particule) – matière (atome cible) »
A la suite de collisions avec les atomes cibles du milieu traversé, des électrons délivrés lors d’une radiation de type β- interagissent avec les électrons ou le noyau de ces atomes.
interaction électron – électron :
Deux cas de figure peuvent se présenter :
Remarque : EL – EM correspond à la différence des énergies de liaison entre les couches électroniques L et M dans cet exemple.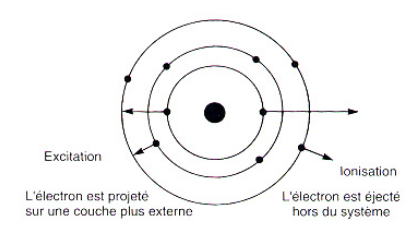
interaction électron – noyau :
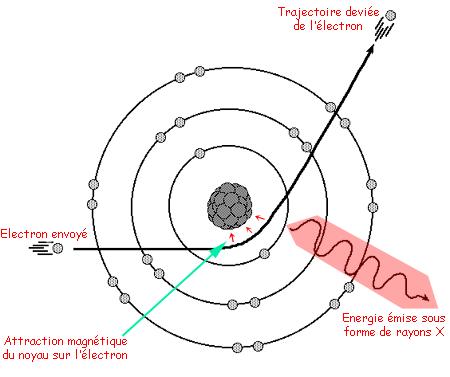
Lorsque l’électron incident passe à proximité d’un noyau, il subit un freinage liée à une force d’attraction exercée par le noyau chargé positivement. L’énergie cinétique perdue lors de ce freinage s’accompagne de l’émission de rayons X. Ce phénomène peut ainsi se répéter jusqu’à dissipation totale de l’énergie cinétique initiale.
3) Conséquences des radiations sur deux molécules fondamentales présentes dans toutes nos cellules : l’eau et l’ADN.
► L’ADN :
Chaque brin d’ADN est composé d’une suite de nucléotides comprenant chacun une base azotée (adénine, thymine, cytosine ou guanine), un sucre cyclique à 5 carbone et un groupement phosphate. En fonction de l’énergie transmise, une irradiation peut engendrer tout d’abord des ruptures de liaison. Ce qui peut entraîner des cassures des brins d’ADN ou la perte de bases azotées. D’autre part, une irradiation peut créer de nouvelles liaisons. Ainsi, une base peut s’associer à une nouvelle molécule ou à une autre base. On parle alors de pontage.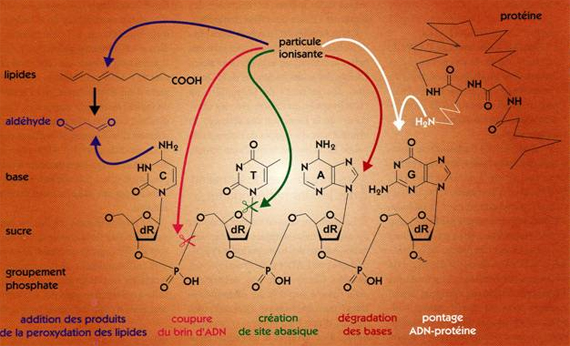 Le nombre et le type de lésions dépendent de l’énergie déposée dans les tissus par les rayons ionisants. En radiothérapie, la « dose de rayonnement » reçue s’exprime en « grays » (Gy). Un gray correspond à une énergie de 1 joule absorbée par 1 kilogramme de matière.
Le nombre et le type de lésions dépendent de l’énergie déposée dans les tissus par les rayons ionisants. En radiothérapie, la « dose de rayonnement » reçue s’exprime en « grays » (Gy). Un gray correspond à une énergie de 1 joule absorbée par 1 kilogramme de matière.
D’après les informations publiées sur le site de la faculté de médecine de Montpellier, une dose de 1 Gy reçue au sein de l’ADN d’une cellule entraîne :
► La radiolyse de l'eau :
L’essentiel de la matière biologique est représenté par l’eau (70% de la masse du corps d’un adulte). Sous l’effet des rayonnements ionisants, la molécule d’eau se dissocie en moins de 10-12 s pour former des radicaux libres. On parle alors de radiolyse.
Un radical libre est une espèce chimique (atome, molécule, fragment de molécule) comportant un ou plusieurs électrons non appariés sur sa couche externe. La règle de l’octet n’est alors pas respectée. La présence d’électron(s) célibataire(s) confère à ces espèces chimiques une grande instabilité et donc une haute réactivité avec d’autres molécules le plus souvent non spécifiques.
Ces radicaux libres tendent à capturer un électron afin de restabiliser leur cortège électronique en un temps très court.
Suivant l’énergie transférée par les radiations aux molécules d’eau, on peut assister à :
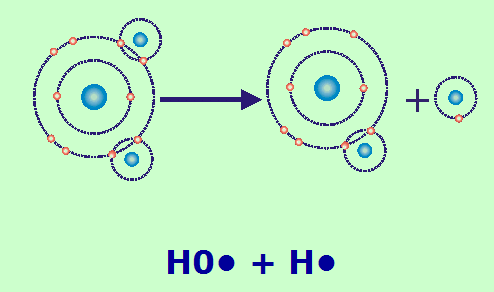
H2O rayonnement e- + H2O+ (dissociation ionique) HO- + H+
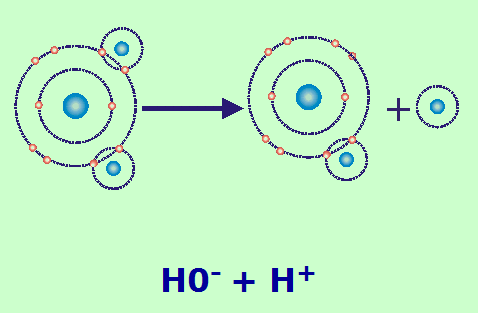

Ces espèces sont toxiques non seulement parce qu’elles sont hautement réactives (radicaux libres) mais aussi parce qu’elles sont oxydantes (peroxyde d’hydrogène).
H2O rayonnement H2O* (molécule d’eau excitée)
4) Effets biologiques des rayonnements ionisants
La radiolyse est un facteur destructeur du fonctionnement cellulaire, car la plupart des processus du vivant dépendent de l’eau ou impliquent la participation de molécules d’eau. La radiolyse de l’eau va entraîner la formation de nombreux radicaux libres qui vont hautement réagir avec les lipides, les protéines, l’ADN… des cellules. Ces réactions vont donc modifier les propriétés des molécules engagées dans ces réactions. La structure et le métabolisme cellulaire vont alors être fortement impactés.
Ce premier phénomène est amplifié par les lésions subies directement par l’ADN lors de son irradiation. Si la cellule ne répare pas ces altérations, la succession des nucléotides et la structure en double hélice de l’ADN se trouvent alors modifiées. Des mutations surviennent. La lecture et l’expression du code génétique sont alors perturbées ou bloquées. Ce qui conduit le plus souvent à l’activation de gènes impliqués dans le phénomène d’apoptose (mort cellulaire programmée).
Le schéma suivant permet de résumer schématiquement ces deux modes d’action associés :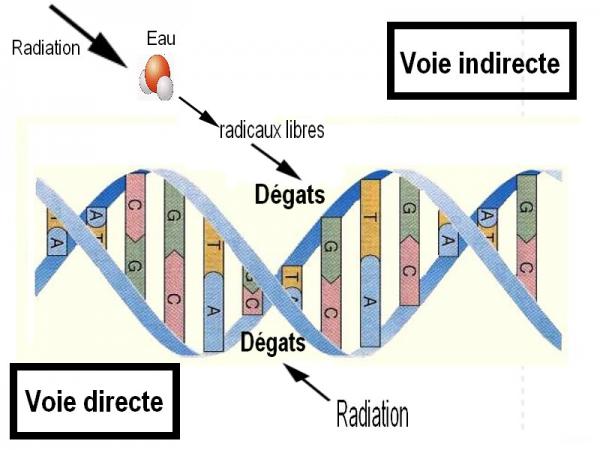
C'est précisément grâce à ces propriétés que les rayonnements ionisants sont utilisés pour détruire les cellules cancéreuses.
Remarque : La radiothérapie produit des effets biologiques aussi bien sur les tissus sains que tumoraux. La capacité de réparation de ces lésions est plus importante pour les premiers que pour les seconds. L'efficacité de la radiothérapie est donc basée sur cet effet différentiel.
5) Des effets biologiques différents suivant le type de rayonnement
Au sein des tissus vivants, le parcours des rayonnements ionisants varie suivant le type et l’énergie des radiations émises.
Les particules (α, électrons…) sont freinées à chaque collision. Quand la particule devient lente en fin de parcours, elle passe davantage de temps pour traverser un atome. Elle a donc plus de chances d'interagir et de l’ioniser à ce moment-là. L’ionisation des tissus devient donc plus intense à la fin du trajet de ces particules.
En revanche, les photons (X, γ…) vont avoir des parcours plus longs et plus pénétrants. En effet, ils n’ont ni masse ni charge. Ils ne subiront donc pas de freinage mais des absorptions successives. L’ionisation des tissus s’étalera donc plus régulièrement sur le parcours.
| Alpha α | Electron β- | X | Gamma γ | |
| Charge électrique | + 2 | - 1 | neutre | neutre |
| Parcours dans les tissus vivants | 50 µm | 5 mm | > 30 cm | > 50 cm |
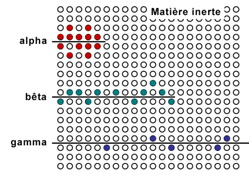
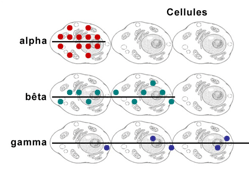
Ces deux derniers schémas confirment que le nombre et la répartition des ionisations au sein des cellules varient suivant la nature et l’énergie des radiations. Par exemple, sur un parcours de 1 µm dans un tissu vivant, une particule alpha de 5 MeV va provoquer 3300 ionisations, un électron de 1 MeV va provoquer 10 ionisations tandis que des rayons X et gamma ne vont créer que quelques ionisations.